Définitions :
Un corps physique peut prendre 3 états :
Solide, liquide ou gazeux.
Chaque passage d'un état à l'autre s'appelle changement d'état.
Solide, liquide ou gazeux.
Chaque passage d'un état à l'autre s'appelle changement d'état.
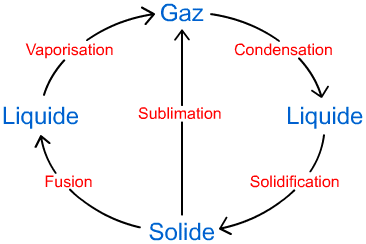
La fusion :
| C'est le passage de l'état solide à l'état liquide. Ce changement d'état s'obtient en apportant de la chaleur au corps que l'on désire faire changer d'état. Pour l'eau, on dira que la glace fond. |
La vaporisation :
| C'est le passage de l'état liquide à l'état gazeux. Ce changement d'état s'obtient en apportant de la chaleur au corps que l'on désire faire changer d'état. Pour l'eau, on dira qu'elle bout. |
La condensation :
| C'est le passage de l'état gazeux à l'état liquide. Pour réaliser ce changement d'état, le corps doit céder de la chaleur. |
La solidification :
| C'est le passage de l'état liquide à l'état solide.Pour réaliser ce changement d'état, le corps doit céder de la chaleur. On dira pour l'eau qu'elle gèle. |
La sublimation :
| C'est le passage direct l'état solide à l'état gazeux sans passer par l'état liquide. Pour réaliser ce changement d'état, le corps doit prendre de la chaleur au milieu ambiant. ce changement d'état s'obtient dans des conditions de pression et de température particulières. Le coprs le plus connu qui réalise ce changement d'état est la naphtaline (boule anti-mîtes). |
Exemple de l'eau :
Si nous partons d'un bloc de glace de 1kg à -20°C, sous pression atmosphérique, et que nous le chauffons. Nous allons rencontrer plusieurs étapes fondamentales dans la transformation de ce bloc de glace...
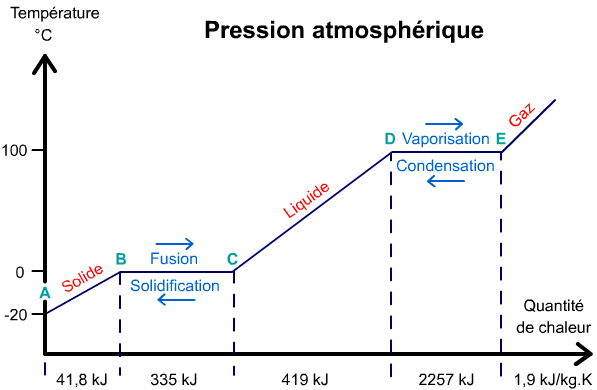
De A à B :
La température de la glace augemente régulièrement pour atteindre 0°C. La chaleur apportée et nécessaire à cette étape est de 41,8 kJ. C'est de la chaleur sensible (la température augmente).
En B :On a un bloc de glace de 1kg à 0°C.
De B à C :
A 0°C, la 1ère goutte de liquide apparaît et la glace commence à fondre. Pendant toute la fonte de la glace, le mélange liquide/solide aura une température rigouresement égale à 0°C. La chaleur apportée est de 335 kJ, c'est de la chaleur latente (la température reste constante).
En C :
On a 1kg d'eau entièrement liquide à 0°C.
De C à D :
La température de l'eau s'élève progressivement jusqu'à atteindre 100°C. Pour réaliser cette augmentation de température, nous devons apporter 419 kJ. C'est de la chaleur sensible.
En D :
On a 1kg d'eau entièrement liquide à 100°C, c'est du liquide saturé.
De D à E :A 100°C, comme nous continuons à apporter de la chaleur, l'eau se met a bouillir et la première molécule de vapeur apparaît. C'est le début de l'évaporation. La température reste constante pendant tout le changement d'état. Quand la dernière goutte de liquide s'évapore, le changement d'état sera terminé, nous aurons apporté 2257 kJ de chaleur latente.
En E :Nous avons 1kg de vapeur à 100°C, c'est de la vapeur saturée.
Après E :
Si on continue à chauffer la vapeur, la tempéraure continue d'augementer nécessitant 1,9 kJ/kg.K.
La température de la glace augemente régulièrement pour atteindre 0°C. La chaleur apportée et nécessaire à cette étape est de 41,8 kJ. C'est de la chaleur sensible (la température augmente).
En B :On a un bloc de glace de 1kg à 0°C.
De B à C :
A 0°C, la 1ère goutte de liquide apparaît et la glace commence à fondre. Pendant toute la fonte de la glace, le mélange liquide/solide aura une température rigouresement égale à 0°C. La chaleur apportée est de 335 kJ, c'est de la chaleur latente (la température reste constante).
En C :
On a 1kg d'eau entièrement liquide à 0°C.
De C à D :
La température de l'eau s'élève progressivement jusqu'à atteindre 100°C. Pour réaliser cette augmentation de température, nous devons apporter 419 kJ. C'est de la chaleur sensible.
En D :
On a 1kg d'eau entièrement liquide à 100°C, c'est du liquide saturé.
De D à E :A 100°C, comme nous continuons à apporter de la chaleur, l'eau se met a bouillir et la première molécule de vapeur apparaît. C'est le début de l'évaporation. La température reste constante pendant tout le changement d'état. Quand la dernière goutte de liquide s'évapore, le changement d'état sera terminé, nous aurons apporté 2257 kJ de chaleur latente.
En E :Nous avons 1kg de vapeur à 100°C, c'est de la vapeur saturée.
Après E :
Si on continue à chauffer la vapeur, la tempéraure continue d'augementer nécessitant 1,9 kJ/kg.K.
Evolution des températures de changements d'état en fonction de la pression :
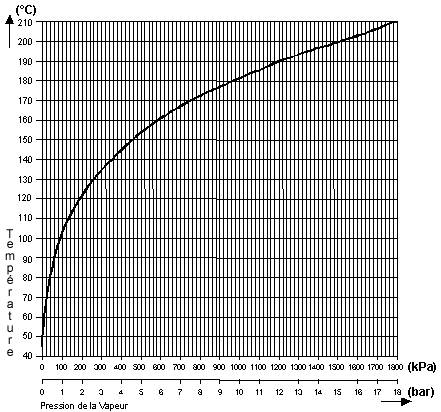
Plus la pression est élevée et plus la tempéraure du changement d'état augemente.
Exemple : à 1,5 bar l'eau bout à 110°C
Exemple : à 1,5 bar l'eau bout à 110°C
Notion d'enthalpie :
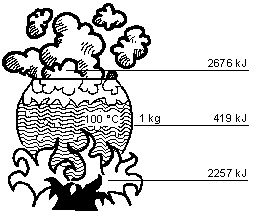
Nous avons vu qu'il fallait apporter 2257 kJ de chaleur à l'eau pour l'évaporer et donc la convertir en 1kg de vapeur à 100°C. Si nous ajoutons les 419 kJ nécessaires pour chauffer 1kg d'eau de 0 à 100°C, on obtient alors 2676 kJ, la teneur en chaleur ou en enthalpie d'1 kg de vapeur saturée à 100°C. (Le point 0 de l'échelle d'enthalpie est fixé à une température de matière de 0°C).
Notion de surchauffe :
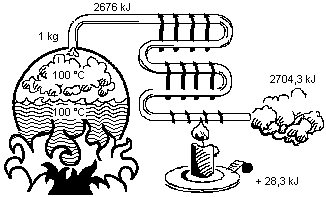
Si nous ajoutons de la chaleur à la vapeur saturée sèche à 100°C, il se produit une augmentation de température appelée surchauffe. La chaleur de surchauffe est de la chaleur sensible. pour augmenter 1kg de vapeur sèche à 100°C de 15K, on doit fournir 28,3 kJ. L'enthalpie de cette vapeur d'eau à 115°C est de 2676+28,3=2704,3 kJ.
Notion de sous-refroidissement :
De même si on extrait de la chaleur à de l'eau qui vient de se condenser, on la sous-refroidit. Ainsi sous pression atmosphérique, de l'eau à 80°C est sous-refroidit de 20°C.
L'enthalpie de l'eau à 80°C est de :
h = 419-20x419/100 = 335,2 kJ/kg.
L'enthalpie de l'eau à 80°C est de :
h = 419-20x419/100 = 335,2 kJ/kg.



ليست هناك تعليقات:
إرسال تعليق